Travere Therapeutics は、Filspari(sparsentan)が巣状分節性糸球体硬化症(FSGS)患者を対象とした第III相DUPLEX試験で、有効性が不十分であったことを発表しました。
「本試験で主要評価項目を達成できなかったことは残念ですが、Filspariの良好な傾向を示す結果が得られたため、FSGSにおける今後の可能性をさらに検討します」
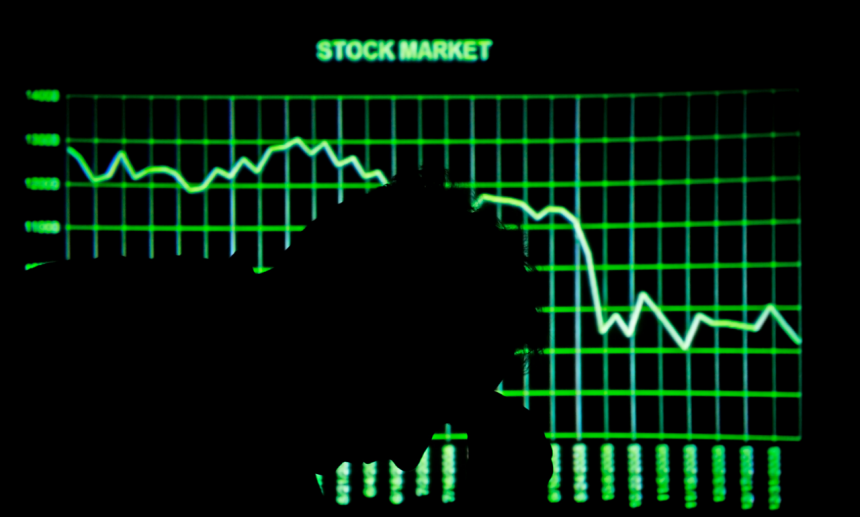
と、CEOのEric Dubeは述べています。とCEOのEric Dubeは述べています。「トップラインの結果を受けて、5月2日に当社株価は35%も下落しました。
アンジオテンシン受容体拮抗薬とエンドセリン受容体拮抗薬の2つの作用を持つ1日1回投与の経口剤は、米国で、急速に病勢が進行するリスクのある原発性IgA腎症の成人におけるタンパク尿の減少に役立つという加速承認を得てから数ヵ月後の後退となりました。
同社は、FSGSの適応追加を希望しており、2021年にDUPLEX試験の中間データとして、Filspariが36週間後に蛋白尿の部分寛解(FPRE)において統計的に有意な反応を示したことを報告した。
DUPLEX試験では、原発性FSGSの患者さん371名を募集し、Filspariを投与する群とイルベサルタンによるアクティブコントロールの群に無作為に割り付けました。
本試験では、米国および欧州における主要評価項目である推定糸球体濾過量(eGFR)total slopeおよびeGFR chronic slopeをそれぞれ測定しました。
Travere社によると、108週間の投与後、Filspariはイルベサルタンと比較して、eGFR総勾配で年間0.3mL/min/1.73m2、eGFR慢性勾配で年間0.9mL/min/1.73m2の好ましい差を示したが、これは統計的に有意ではなかった。
Travere社は、腎臓の転帰を含む副次評価項目およびトップラインの探索的評価項目は、同社の薬剤にとって「好ましい傾向」であると述べまして。
108週後、尿蛋白/クレアチニン比(UP/C)のベースラインからの変化は、フィルスパリで50%、イルベサルタンで32%。また、108週目にFPREを達成した患者は、フィルスパリ投与群で38%、対照群では23%であった。
UP/Cが0.3g/g未満と定義される蛋白尿の完全寛解は、両群でそれぞれ18%、7%の患者に認められました。
Travere社によると、安全性に関する予備的な検討の結果、Filspariの忍容性は概して良好であり、治療群間で全体的な安全性プロファイルは同様であったとのことです。
参照
Travere Therapeutics Announces Topline Results from (globenewswire.com)
あわせて読みたい
- 【クラリベイトが選ぶ】2023年最も「注目するべき医薬品15選」徹底解説|その理由と最新ニュースのまとめ
- 海外製薬ニュースの使い方【完全ガイド】メリットから活用方法まで徹底解説
- 無料メルマガ「1分でわかる海外製薬ニュース」登録はこちらから
- 【製薬業界の転職】転職エージェントの選び方は「複数登録」がオススメ|失敗しない方法を徹底解説